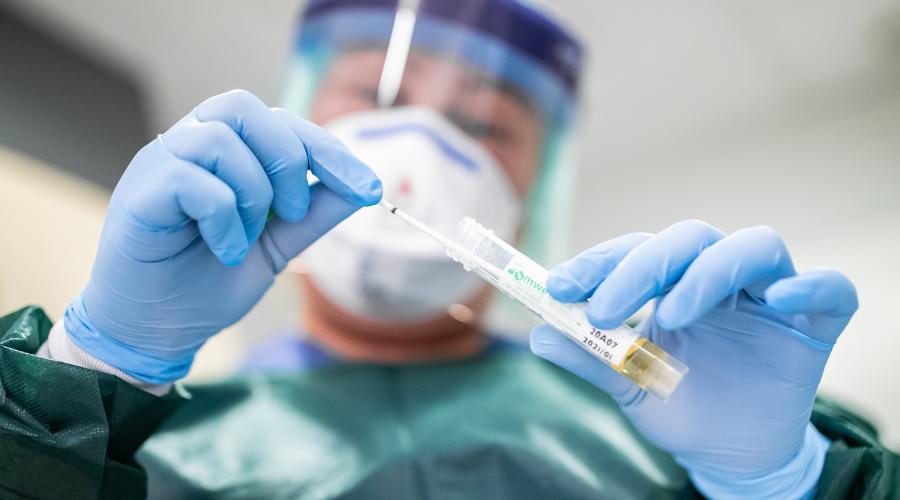
بررسی روشهای تشخیصی مولکولی SARS-CoV2
منبع انتشار : دکتر سید مهدی افتخاری - دکتر سید امین افتخاری
در این نوشتار سعی میکنیم به بررسی روشهای تشخیصی مولکولی SARS-CoV2 که تاکنون در دسترس هستند بپردازیم. این ویروس در اواخر سال 2019 میلادی از شهر ووهان چین شروع به انتشار کرد و بهسرعت تمام دنیا را در برگرفت. با توجه به اهمیت تشخیص بهموقع ویروس در کنترل بیماری، شرکتهای تحقیقاتی نیز بهسرعت کیتهای آزمایشگاهی مولکولی را طراحی و در دسترس آزمایشگاهها قرار دادند.
ویروس SARS-CoV2 جزو خانواده ویروسهای RNA دار میباشد. ویروس در نواحی اپیتلیوم اروفارنکس، نازوفارنکس و مخاط بینی در ابتدا شروع به تکثیر کرده و سپس وارد جریان خون میشود. هرچند دوره ویرمی ویروس در جریان خون کوتاه میباشد و بنابراین نمونه مورد استفاده برای شناسایی عفونت باید از مخاط حلق و بینی و در برخی شرایط از مجاری تنفسی تحتانی انجام شود.
تأیید تشخیص عفونت بر پایه شناسایی ماده ژنومی ویروس یا همان RNA ویروس میباشد، که با استفاده از تکثیر ژن ویروسی با تکنیک RT-PCR میباشد. نواحی مختلف ژنوم ویروس برای تکثیر در نظر گرفته شده است که شامل ژنهای Envelope (e)، نوکلئوکپسید (N) و RNA dependent RNA polymerase (RdRp) میباشد. سازمان جهانی بهداشت در پروتکل در مورخ 17 ژانویه 2020، از ژن e جهت خط اول غربالگری و از ژن RdRp جهت تأیید تشخیص نام برده است. سازمانهای علمی که در این زمینه کار میکنند بر این باور هستند که درصورتیکه بیمار از نظر ژن e مثبت شد و میزان بار ویروسی بالا باشد (ct<38) نیازی به بررسی ژن تأییدی نمیباشد ولی در صورتی نتیجه بینابینی باشد (ct>38) باید با بررسی ژن RdRp نتیجه تأیید شود. کلیه کیتهای تولیدی بهعنوان کنترل استخراج و صحت انجام واکنش PCR، یکی از ژنهای انسانی را که بهطور طبیعی در سلولهای اپیتلیال مخاط تنفسی قرار دارد را همراه با ژن ویروسی بررسی میکنند. از این ژن بهعنوان کنترل داخلی یاد میشود که در حال حاضر ژن RNAase P مورد استفاده قرار میگیرد. بدیهی است که درصورت منفی شدن نتیجه ژن RNAase P، آزمایش و نمونهبرداری باید تکرار شود. هر یک از شرکتهای تولیدکننده، یک و یا ترکیبی از پروب های فوق را جهت کیتهای تولیدی خود انتخاب کردهاند. بهعنوانمثال پروب های تولیدشده توسط مرکز کنترل و پیشگیری بیماریهای آمریکا (CDC) بر پایه نوکلئوکپسید هستند. کیتهای ساخت داخل هم نیز بر پایه پروب های ژن N و RdRp طراحیشدهاند.
روش RT-PCR نیازمند استخراج مولکول RNA میباشد. از طرفی تکثیر ویروس نیز زمانبر میباشد. همچنین حین انجام پروسه تکثیر ژن در دستگاه PCR نمیتوان نمونه جدیدی به دستگاه داد. بنابراین جوابدهی نسبتاً طولانی میباشد (حداقل 24 ساعت). بنابراین برخی شرکتها دست به طراحی روشهایی برای تکثیر ژن کردند که یا نیازی به جداسازی RNA به روشهای مرسوم نداشته و یا اینکه کلیه مراحل استخراج و تکثیر در یک کارتریج بهطور مجزا انجام میگیرد. بهطورکلی این روشها تحت عنوان روشهای بر بالین بیمار (POC) شناخته میشوند. ازجمله این شرکتها، شرکت Abbott آمریکا میباشد که از تکنیک isothermal amplification برای تکثیر ژنوم استفاده میکند. تکثیر ژنوم در این روش نیازی به تغییر دما ندارد. هرچند در این روش تنها یک ژن قابلیت تکثیر داشته و لذا بررسی ژن کنترل داخلی و بررسی همزمان چندین ژن برای بالا بردن حساسیت تشخیصی امکانپذیر نمیباشد.
شرکت GeneXpert آمریکا نیز کیتی بر پایه روش RT-PCR بر روی دستگاه Cepheid طراحی نموده که کلیه مراحل استخراج و تکثیر ژن در داخل یک کارتریج انجام میگیرد. بنابراین امکان آلودگی محیط و انتقال ویروس به سایر افراد در این روش بهشدت کاهش مییابد. تکثیر ویروسی در این کیت بر پایه ژن e و N میباشد. بعلاوه کنترل داخلی نیز جهت تأیید مراحل در کیت قرار داده شده است. شناسایی ویروس با این دستگاه طی 45 دقیقه در هر زمانی از شبانهروز قابل انجام میباشد. این سیستم در حال حاضر در ایران موجود میباشد و شرکت ایرانی دارای نمایندگی این دستگاه در حال کسب تأییدیههای لازم از وزارت بهداشت جهت واردات کیت میباشد.
در پایان لازم است آگاه باشیم که با وجود دقت و حساسیت بالای روشهای مولکولار برای شناسایی عوامل بیماریزا، در تمام این روشها ویروس و عامل عفونی باید در نمونه موجود باشد که با توجه به نمونهگیری مشکل در بیماری COVID-19 بعضاً نمونهگیری از محل مناسب انجام نگرفته که باعث منفی شدن نتیجه با وجود بیماری در فرد میشود. لذا در تفسیر نتایج حتماً باید شرایط بالینی بیمار و نتایج تستهای رادیولوژیک بیمار نیز مدنظر قرار گیرد. ولی درصورتیکه نمونهگیری بهطور صحیح انجام شود، این روشها میتوانند حتی افراد در دوران اولیه بیماری (کمون) که فاقد علائم بالینی هستند را نیز شناسایی کنند.